1。原子の再配列
* 債券が破壊されます: 反応物に原子を結合している化学結合は壊れています。これには、エネルギー入力が必要です。
* ボンドフォーム: 原子の間に新しい結合が形成され、製品が作成されます。このプロセスはエネルギーを放出します。
2。エネルギーの変化
* 発熱反応: 彼らが吸収するよりも多くのエネルギーを放出し、その結果、周囲にエネルギーを正味放出します。製品は反応物よりもエネルギーが低い。
* 吸熱反応: 放出よりも多くのエネルギーを吸収し、周囲からのエネルギーの正味吸収をもたらします。製品は反応物よりも高いエネルギーを持っています。
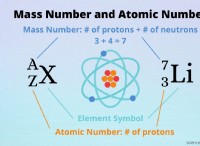
3。質量の保全
* 質量保存法則: 反応前の反応物の総質量は、反応後の生成物の総質量に等しくなければなりません。原子は作成も破壊もありませんが、単に再配置されます。
4。化学的性質の変化
* 新しい物質: 製品は、反応物とは異なる化学的特性を持っています。それらは根本的に異なる物質です。
5。活性化エネルギー
* エネルギー障壁: 化学反応は、発熱性であっても、開始するために一定量のエネルギー(活性化エネルギー)が必要です。このエネルギーは、既存の結合を破り、反応を開始するのに役立ちます。
覚えておくべきキーポイント:
* すべての反応が見えるわけではありません: 多くの化学反応は分子レベルで発生し、私たちの感覚には明らかではありません。
* 反応率は異なります: 反応は、温度、濃度、触媒の存在などの要因の影響を受け、さまざまな速度で発生します。
* 可逆性: いくつかの反応は両方向に進むことができ、反応物は産物を形成し、その逆も同様です。
化学反応の特定の側面をより深く掘り下げたい場合はお知らせください!