その理由は次のとおりです。
* 電気陰性度: 炭素と硫黄は、同様の電気陰性度値を持っています。 これは、電子を引き付ける能力が同様の能力を持っていることを意味します。
* 電子の共有: 一方の原子が他の原子から完全に電子を採取する代わりに、それらは電子を共有して安定した外側のシェルを実現します。この共有は共有結合をもたらします。
特定の例:
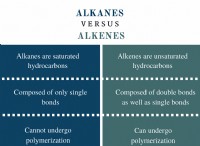
* ジスルフィド炭素(CS2): 炭素と硫黄の原子は二重結合で接続されています。
* Thiols(r-sh): チオールでは、硫黄原子は単一の結合を介して炭素原子に結合されます。
共有結合の詳細情報が必要な場合はお知らせください!