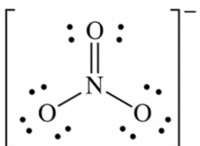
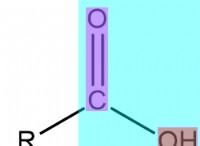
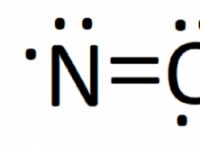* 酸: 溶液中に水素イオン(H+)を生成する物質。一般的な例には、塩酸(HCl)、硫酸(H2SO4)、酢酸(CH3COOH)が含まれます。
* ベース: 溶液中に水酸化物イオン(OH-)を生成する物質。一般的な例には、水酸化ナトリウム(NaOH)、水酸化カリウム(KOH)、および水酸化カルシウム(Ca(OH)2)が含まれます。
中和反応は、酸と塩基が互いに反応して塩と水を形成するときに発生します。
これは、反応を表す単純化された方程式です。
酸 +ベース→塩 +水
例えば:
hcl(酸) + naOH(ベース)→NaCl(塩) + H2O(水)
この特定の例では、形成された塩は一般にテーブル塩として知られている塩化ナトリウムです。