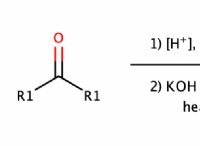
* ルイス構造: 中央の酸素原子には、フッ素原子に2つの単一結合があり、2つの孤立した電子ペアがあります。
* vsepr理論: VSEPR(Valence Shell Electron Pair Repulsion)理論は、電子ペア(結合と非結合の両方)が反発を最小限に抑えるために自分自身を整理すると予測しています。 o₂f₂では、中央の酸素原子の周りの4つの電子ペアが四面体形状に配置されています。
* 分子形状: 酸素原子の唯一のペアは、結合ペアよりも強い反発を行い、フッ素原子を近くに押し込みます。これにより、曲がったまたは角度分子幾何学が生じます。
要約: o₂f₂には四面体電子ペアの形状がありますが、中心酸素原子に対する孤立ペアの影響により、その分子形状は曲がっています。