原子核から中性子を除去または追加すると、生成される物質は同じ元素の新しいタイプであり、同位体と呼ばれます。
身の回りにあるものはすべて物質でできており、すべての物質は原子でできています。原子をさらに分解することはできますか?絶対。原子は、陽子、中性子、電子、および私たちのほとんどが気付いていないさまざまな素粒子の束で構成されています。
では、すべてが原子で構成され、原子自体が亜原子粒子で構成されている場合、亜原子粒子の組み合わせを変更すると、新しい異なる種類の物質が生じるでしょうか?
原子から電子を取り除くと、正に帯電したイオンが残り、別の反対に帯電したイオンと結合する準備が整います。陽子が取り出されたり、原子に追加されたりすると、まったく新しい元素が形成されます (原子核を安定に保つために、同じ数の中性子を追加または削除する必要もあります)。しかし、原子核から中性荷電中性子を取り除くとどうなるでしょうか?おそらく新しい要素でしょうか?
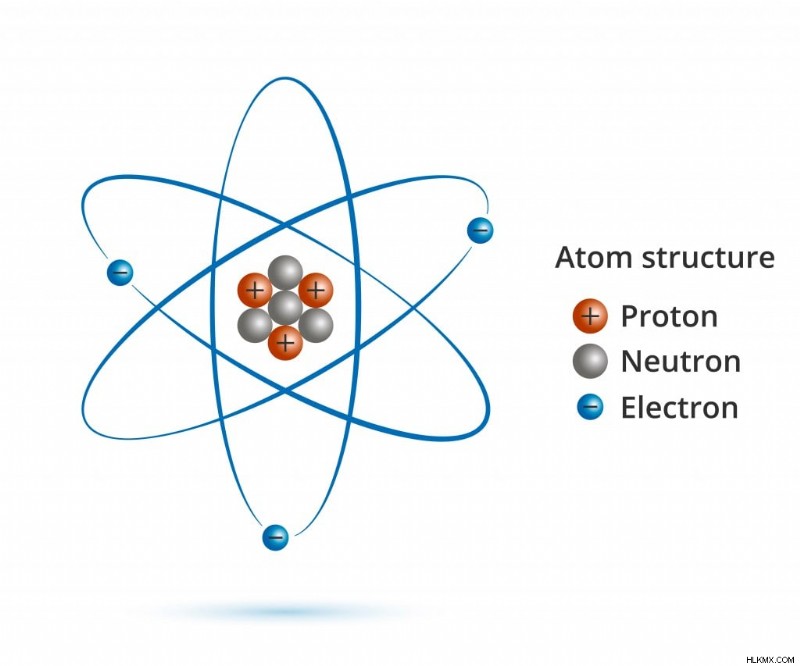
原子には、主に陽子、電子、中性子が含まれています。これらの粒子のいずれかを追加または削除すると、原子の特性とアイデンティティが変更されます。 (写真提供:Vector FX/Shutterstock)
同位体
原子核から中性子を削除または追加すると、技術的には新しい元素を取得するわけではありませんが、同じ元素の新しいタイプが手に入ります。この新しいタイプは、元素の「同位体」と呼ばれます。同位体は、陽子の数は同じですが、核内の中性子の数が異なる元素として正式に定義されています。同位体の別の定義では、原子番号 (陽子の数) は同じですが、原子質量数 (原子の中性子と陽子の合計) が異なる原子として定義されています。元素の同位体も同じ数の電子を持っています。
さて、新しく発売された iPhone を使って、同位体の概念をより身近な方法で理解しましょう。 Apple は最近、Apple iPhone シリーズの 3 つの新しいデバイス、すなわち iPhone 11、iPhone 11 Pro、iPhone 11 Pro Max をリリースしました。 Pro と Pro Max は、iPhone 11 の異なるバリアントまたはタイプにすぎません。この 2 つは、同じ A13 Bionic チップを使用しているため、または単に 2019 年にリリースされたという理由で、iPhone 11 のタイプとして識別される可能性があります。
すべての元素は、原子番号、つまり核内の陽子の数だけに基づいて識別されます。そのため、iPhone と同様に、陽子の数が同じ (A13 チップを搭載した iPhone) で中性子の数が異なる (カメラの数またはバッテリーのサイズが異なる) 要素は、同じ要素の異なるタイプとして識別されます。まったく新しい要素です。
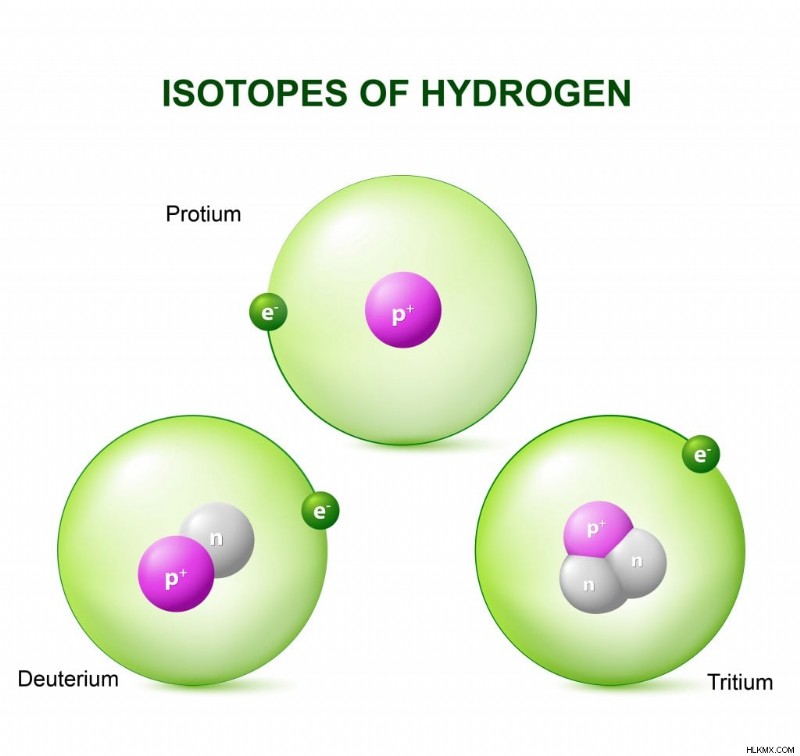
水素には自然界に存在する 3 つの同位体があり、それぞれが他よりも多くの中性子を持っていますが、陽子の数は同じです。 (写真提供:Designua/Shutterstock)
同位体の歴史
放射性同位体の存在は、放射性カスケード (一連の放射性崩壊) を研究している 1913 年に、放射化学者の Frederick Soddy によって最初に認識されました。 Soddy は、ウランと鉛の間に 40 の異なる元素種 (放射性元素と呼ばれる) を発見しました。しかし、周期表では、この 2 つの間に 11 の元素しか認められていませんでした。これらの 40 元素を周期表に配置しようとして、Frederick Soddy と Kazimierz Fajans は放射性変位理論を思いつきました。
この理論では、アルファ崩壊 (原子がヘリウム原子核、つまり 2 つの陽子と 2 つの中性子を放出する放射性崩壊) は、周期表で親元素の 2 つ左にある元素を生成するのに対し、ベータ崩壊 (原子核の放出) は、電子または陽電子) は、親の 1 つ右の要素になります。
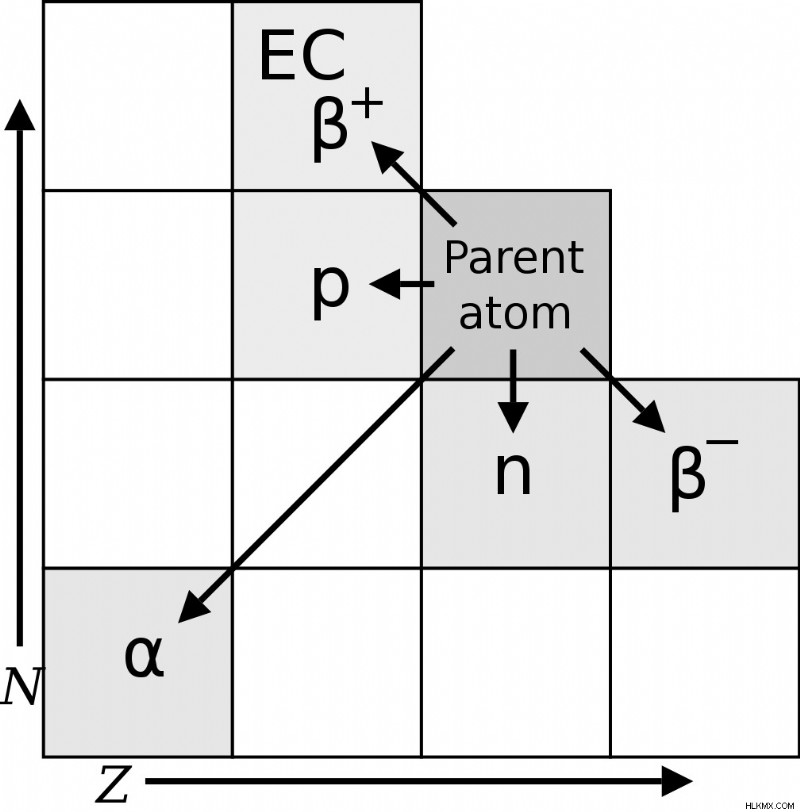
各タイプの崩壊に続いて形成される要素の視覚的表現。ここで、N は中性子の数、Z は原子番号を表します。 (写真提供:MarsRover/Wikimedia Commons)
しかし、ソディは、いくつかの放射性元素は異なる原子量/質量を持っていても、親元素の化学的性質を保持しているため、周期表で同じ場所を占める必要があることに気付きました. Frederick Soddy の友人である Margaret Todd は、これらの放射性元素の「同位体」という用語を作り出しました。同位体という言葉はギリシャ語で「同じ場所」を意味します。ソディは、放射性元素の理解と同位体の調査と発見への貢献により、1921 年にノーベル化学賞を受賞しました。 J. J. トムソンは、1913 年に元素の最初の安定同位体を発見しました。
同位体間の特性の違い
簡単にするために、元素の特性を化学的特性と物理的特性の 2 つの部分に分けることができます。化学的性質は、化合物や他の元素を形成する化学反応を起こす元素、つまりその原子の能力と傾向です。これらの特性は、原子に存在する電子の数によって決まります。元素の同位体は中性子の数が異なりますが、電子の数は同じであるため、化学的性質は似ています。ただし、水素の同位体は例外です。
一方、元素の沸点や融点などの物理的性質は、その原子質量数に依存します。質量数の違いは、親からの同位体に異なる物理的性質を与えます。ただし、同位体の核特性は互いに異なり、それらの分類の基礎も形成します。
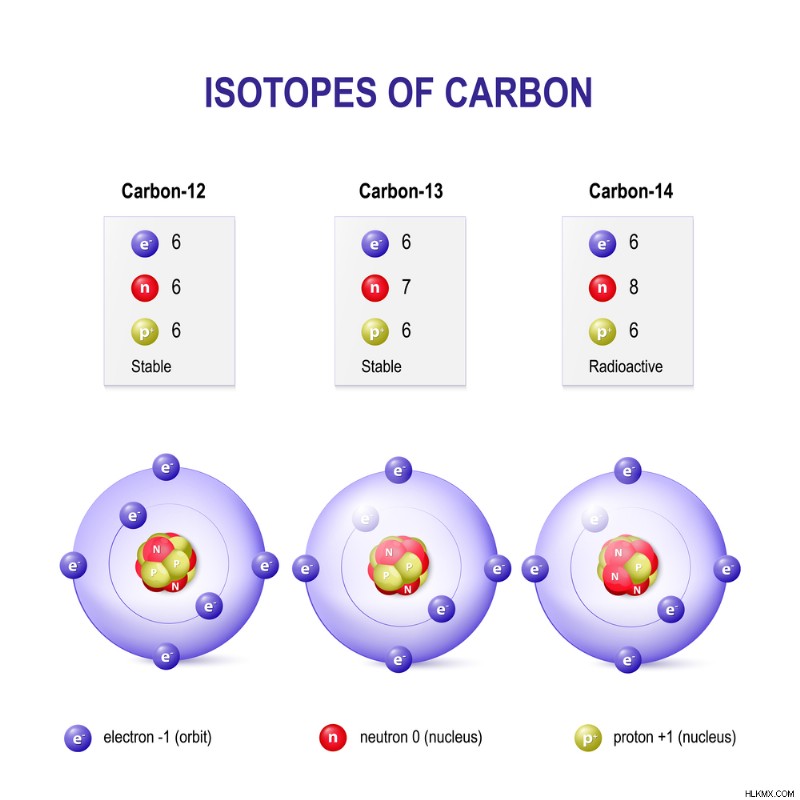
炭素には、天然に存在する 3 つの同位体があります。炭素 12 と炭素 13 は安定同位体ですが、炭素 14 は放射性です。 (写真提供:Designua/Shutterstock)
同位体は、その安定性または崩壊傾向に基づいて分類されます。天然に存在する 339 の同位体のうち、約 252 が安定していると考えられています。ただし、実際に安定しているのは 146 個だけで、残りの 106 個は理論上 腐敗しやすい。このような観測は今のところ行われていないため、観測的に安定していると考えています。
また、自然界に存在する 339 種類の同位体のうち、286 種類は原始的なもの、つまり太陽系の形成以来存在していたものです。これまでに確認された同位体の総数は、人工的に作成されたものと合わせて 3,300 を超えています。これらのうち 2,400 を超えるものは、半減期が 60 分未満です。すべての元素には 1 つ以上の放射性同位体がありますが、原子番号が 83 を超える元素には放射性同位体しかありません。
結論
これは魅力的なテーマかもしれませんが、原子核から中性子を除去することは簡単なことではありません。同位体は、核反応の副産物として、主に原子炉の使用済みロッドに見られます。それらは、粒子加速器で安定した原子にアルファ粒子(ヘリウム核)を衝突させることによって人工的に生成されます。他の方法には、原子炉内で親同位体に中性子を照射する方法や、サイクロトロンを使用する方法があります。
放射性同位体は、さまざまな分野で使用されています。最も有望なのは、核医学とがんの治療です。産業用途には、国土安全保障、食品照射、産業用放射線写真、地質学、天文学などが含まれます。将来、さらに多くの同位体が発見され続けるため、どのような新しい用途が見つかるかは誰にもわかりません!