なぜ元素が化合物を形成するのか?
要素が組み合わせて化合物を形成します。いくつかの理由:
* 安定性: 原子は、最も外側の電子シェルがいっぱいになると最も安定しています。不完全な外側シェルを持つ要素は、他の要素と反応して完全な外側シェルを実現する傾向があります。これは、より安定した構成です。
* 静電引力: 原子は、反対の電荷間の魅力のために結合を形成できます。これは、原子が電子を獲得または失ったときに発生し、イオン(荷電粒子)の形成をもたらします。
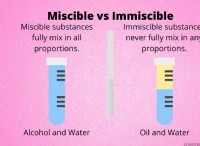
* 電子の共有: 原子は、電子を共有することにより結合を形成することもできます。このタイプの結合は共有結合と呼ばれ、非金属間で特に一般的です。
化合物の種類:
* イオン化合物: 正の帯電イオン(陽イオン)と負に帯電したイオン(アニオン)の間の静電引力によって形成されます。 例:テーブル塩(NaCl)、塩化カルシウム(CACL2)。
* 共有化合物: 原子間の電子の共有によって形成されます。例:水(H2O)、二酸化炭素(CO2)。
要するに
要素は組み合わせて化合物を形成します。なぜなら、電子(イオン結合)を獲得または失うか、電子(共有結合)を共有することにより、より安定した電子構成を実現できるからです。この安定性は、反対に帯電した粒子または共有電子ペアの間の引力から生じます。