基本を理解する
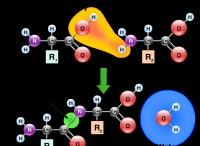
* リン酸ナトリウム緩衝液: この緩衝液は、通常、単菌性リン酸ナトリウム(NAH2PO4)とジバシックリン酸ナトリウム(NA2HPO4)の混合物を使用して作られています。これらの2つのコンポーネントは、共役酸塩基ペアとして機能し、ソリューションがpHの変化に抵抗することができます。
* ph 6.9: バッファの目的のpH。これにより、NAH2PO4と必要なNa2HPO4の比率が決まります。
* 0.006 m NaCl: これは、単にバッファーに追加される塩溶液です。それはバッファーのpHに直接影響するわけではありませんが、特定の実験的ニーズに使用される可能性があります。
バッファーを準備する手順
1。必要な質量を計算します:
* PKA:を決定します リン酸緩衝液に関連するPKAは7.21(H2PO4- / HPO42-平衡のPKA)です。これはあなたの希望のpHに近いため、良い選択になります。
* Henderson-Hasselbalch方程式:を使用します
* ph =pka + log([hpo42-] / [h2po4-])
* 6.9 =7.21 + log([hpo42-] / [h2po4-])
*比率を解く:[hpo42-] / [h2po4-] =0.50
* 各リン酸成分の臼歯を計算します:
*総リン酸塩モル=0.02 m
* [NA2HPO4] =0.02 m *(0.50 / 1.50)=0.0067 m(ほぼ)
* [nah2po4] =0.02 m *(1.00 / 1.50)=0.0133 m(ほぼ)
* モラリティをグラムに変換:
* NAH2PO4(119.98 g/mol)とNa2HPO4(141.96 g/mol)の分子量が必要です。
*次の式を使用して各コンポーネントに必要な質量を計算します:質量=(臼歯 *体積 *分子量) / 1000
*たとえば、NAH2PO4の場合、1 Lのバッファーを作成する場合は次のとおりです。
*質量=(0.0133 mol/l * 1 l * 119.98 g/mol)/1000 =1.59 g
*同様にNa2HPO4の質量を計算します。
2。塩を水に溶かします:
*計算された量のNAH2PO4とNA2HPO4を比較検討します。
*約800 mlの蒸留水に溶解します。
*計算されたNaClの質量を溶液に追加し、溶解して溶解します。
*磁気炒め物または攪拌棒を使用して、徹底的な混合を確保します。
3。 pH(オプション)を調整します:
* pHメーターを使用して、溶液のpHを確認します。
* pHが正確に6.9でない場合、1 M HCl(pHを下げる)または1 M NAOH(pHを上げる)のいずれかを少量追加することで、それをわずかに調整できます。メーターでpHを監視しながら、これらのソリューションを滴下します。
4。最終ボリュームのソリューションを持ち込みます:
* pHが調整されたら、蒸留水を慎重に追加して、溶液の総体積を1 Lにもたらします。
5。チェックと保存:
* PHをもう一度確認して、正しいことを確認してください。
*バッファーを室温で、または冷蔵庫に保管して、より長い保管してください。
重要な考慮事項
* 水の品質: 最高の結果を得るには、高品質の蒸留水を使用してください。
* 精度: 正しいバッファー濃度を確保するために、塩を正確に計量します。
* pHメーターキャリブレーション: 正確な測定に使用する前に、pHメーターを適切に調整します。
* 安全性: 化学物質を扱うときは、常に適切な安全装置(手袋、ゴーグル)を着用してください。
この手順では、0.006 m NaClのpH 6.9で0.02 mのリン酸ナトリウム緩衝液が得られるはずです。別のボリュームのバッファーを作成する必要がある場合は、ボリュームと計算を調整することを忘れないでください。