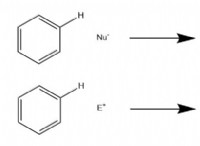
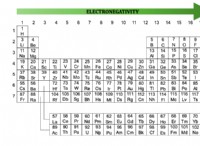
その理由は次のとおりです。
* 水は極性分子です: 水中の酸素原子は、水素原子よりも電気陰性です。つまり、電子をより強く引き付けます。これにより、酸素に部分的な負電荷が生じ、水素に部分的な正電荷が生じ、分子極が発生します。
* イオン化合物は、静電力によって一緒に保持されます: これらの力は強いですが、水のような極地分子によって破壊される可能性があります。水中の部分的に負の酸素は、イオン化合物の陽イオンを引き付け、部分的に陽性の水素は陰イオンを引き付けます。この引力は、イオン化合物を一緒に保持する静電力を弱め、それを溶解させます。
* 極性分子は極性溶媒に溶解します: 水は極性溶媒であり、糖やアルコールなどの他の極性分子を溶解できます。 水分子の部分電荷は、極性分子の部分電荷と相互作用し、それらを溶解させます。
要約: 水の極性により、イオン分子と極性分子の両方と相互作用し、結合を破壊して溶解することができます。