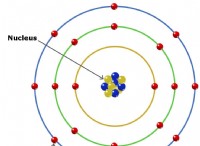
イオン結合 ある原子が電子を別の原子に完全に透過すると発生します。これはイオンを作成します:
* カチオン: 原子が電子を失ったときに形成された正に帯電したイオン。
* アニオン: 原子が電子を獲得したときに形成された負に帯電したイオン。
イオンの反対の電荷は互いに引き付けられ、化合物を形成します。
例を示します:
*ナトリウム(Na)には、その外殻に1つの電子があり、それを容易に失い、正に帯電したナトリウムイオン(Na+)になります。
*塩素(Cl)には、その外殻に7つの電子があり、1つの電子を容易に獲得して、負に帯電した塩化物イオン(CL-)になります。
Na+とCl-イオンの間の引力は、化合物ナトリウム(NaCl)、またはテーブル塩を形成します。
要約:
* 共有結合: 原子間で電子を共有します。
* イオン結合: 原子の間に電子を伝達します。
したがって、共有結合は一般的ですが、すべての化合物が電子を共有することによって形成されるわけではありません 。イオン結合は、多くの重要な化合物の形成において重要な役割を果たします。