その理由は次のとおりです。
* pHスケール: pHスケールは、溶液の酸性度またはアルカリ度を測定します。 7のpHはニュートラルです。 7未満の値は酸性であり、7を超える値は基本(アルカリ)です。
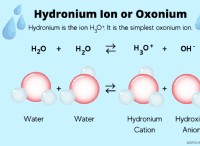
* 水酸化物イオン: 水酸化物イオン(OH-)は、溶液のアルカリ性の原因です。 水酸化物イオンの濃度が高いほど、溶液はより基本的です。
* 水素イオン: 逆に、酸性溶液は水素イオン(H+)の濃度が高くなります。
基本的なソリューションの例:
* 水酸化ナトリウム(NaOH) :一般に灰汁として知られているが、水中で完全に解離して水酸化物イオンを産生する強力なベースです。
* 水酸化カリウム(KOH): 水酸化ナトリウムと同様に、もう1つの強力なベースです。
* アンモニア(NH3): これは、水と反応して水酸化物イオンを形成する弱い塩基です。
重要な注意: 水酸化物イオン(OH-)の形成は、基本的なソリューションの重要な特徴ですが、すべての基本的なソリューションが直接形成されるわけではありません。一部の塩基は水と反応して水酸化物イオンを生成します。