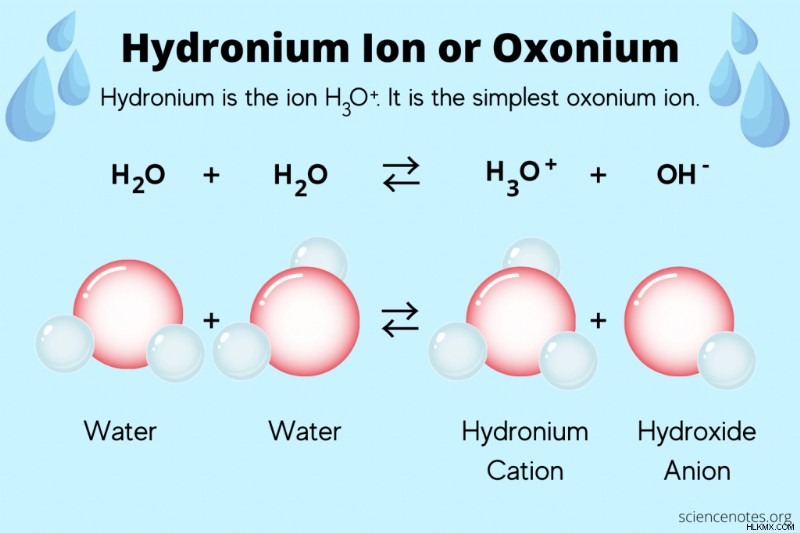
化学では、ヒドロニウム またはヒドロニウムイオン 化学種 H3 を指します O. ヒドロニウムは最も単純なオキソニウム イオンです ここで、オキソニウム イオンは、3 つの化学結合を持つ任意の酸素カチオンです。国際純正応用化学連合 (IUPAC) は、「ヒドロニウム」という言葉の代わりに「オキソニウム」または「ヒドロキソニウム」という用語を使用することを推奨しています。ただし、ヒドロニウムはイオンの一般名のままです。
水中の遊離水素なし
水素イオン (H) は水溶液中の化学式や pH 計算に現れますが、遊離水素イオンは実際には水中を浮遊しません。代わりに、陽子 (水素イオン) の信じられないほど高い正電荷密度により、すぐに 1 つまたは複数の水分子と会合し、ヒドロニウムを形成します。
したがって、水の自動解離の方程式は次のとおりです。
H2 O → H(aq) + OH(aq)
しかし、より正確な化学式はヒドロニウムを示しています:
2 H2 O(l ) ↔ H3 O(aq ) + OH(aq )
ヒドロニウム構造
この方程式でさえ単純化しすぎています。水が自己解離するとき、水素イオンは常に単一の水分子と結合してヒドロニウムを形成するとは限りません。多くの場合、陽子は複数の分子と結合し、ある分子から別の分子へと飛び移ります。同様に、水酸化物イオンは複数の水分子と相互作用します。
冷水では、ヒドロニウム イオンは平均 6 つの水分子と相互作用します。ただし、他の構造が発生します。たとえば、H3 O(H2 O)20 非常に安定した、または「マジックナンバー」構造です。対極にあるツンデル陽イオン (H5 O2 )は、対称水素結合を介して水素を均等に共有する2つの水分子を含みます。 固有陽イオン (H9 O4 ) 3 つの水分子の中心として作用するヒドロニウム イオンがあり、これも水素結合に関係しています。
ヒドロニウム イオン自体は三角錐の形をしており、ピラミッドの頂点に酸素があります。イオンの重心は酸素イオンに近い。結合角 H-O-H は約 113° です。
ヒドロニウムの重要性
ヒドロニウム イオンの概念は、pH 計算、酸塩基化学、および星間化学において重要です。
したがって、pH 式は 2 つの形式を取ります:
pH =-log[H]
pH =-log[H3 O]
水素イオンまたはヒドロニウムイオンは、アレニウス酸の定義の基礎を形成します。したがって、塩酸の解離は次のようになります。
HCl(aq) + H2 O → H3 O(aq) + Cl(aq)
ほとんどの計算では、H を使用するか H3 を使用するかは問題ではありません ああ、しかし、いくつかの興味深い化学には、化合物の陽イオンとして作用するヒドロニウムが含まれていることを知っておく価値があります.たとえば、一部の強酸は、ヒドロニウム塩の結晶を形成します。液体の無水過塩素酸と水を 1:1 の比率で混合すると、固体の過塩素酸ヒドロニウム (H
星間化学では、ヒドロニウムは、拡散および高密度の分子雲、星間物質、および彗星のプラズマ尾部で発生します。通常、これは H2 のイオン化から始まります (水素分子) を H2 に変換 宇宙放射線によって。ただし、いくつかの再結合反応が可能であり、水、ヒドロニウム イオン、水酸化物イオンが形成されます。
参考文献
- Burgot, Jean-Louis (1998). 「Ka○(H3 お、H2 O) と Kb○(H2 O, OH) は水中で対になる」. アナリスト . 123 (2):409–410. doi:10.1039/a705491b
- Herbst, E.;クレンペラー、W. (1973)。 「密集した星間雲における分子の形成と枯渇」. 天体物理ジャーナル . 185:505. doi:10.1086/152436
- IUPAC (1997)。 「オキソニウムイオン」。化学用語集 (「ゴールド ブック」) (第 2 版)。ブラックウェル科学出版物、オックスフォード。 ISBN 0-9678550-9-8。 doi:10.1351/goldbook
- マイスター、エーリッヒ。ウィルケ、マーティン。アングスト、ヴェルナー。トニ、アントニオ。ウォルデ、ピーター(2014)。 「化学教科書におけるブレンステッド・ローリー酸塩基平衡の定量的説明の混乱 - 化学教育者のための批判的レビューと説明」. Helv.チム。アクタ . 97 (1):1–31. doi:10.1002/hlca.201300321
- オラ、ジョージ A. (1998)。 オニウムイオン .ジョン・ワイリー&サンズ. ISBN 9780471148777.