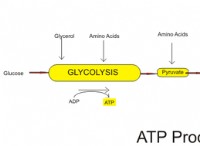
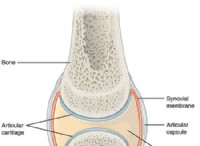
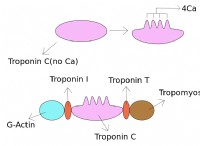
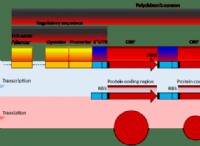
1。分子障害の増加:
* 溶質: 溶質が溶けると、その分子はより分散し、溶媒全体に広がります。これにより、溶質分子の可能な配置が増え、システムのエントロピーが増加します。
* 溶媒: 溶媒分子はまた、溶質と相互作用する際に配置に変化を経験します。この相互作用は、特定の相互作用に応じて溶媒エントロピーの増加と減少の両方につながる可能性があります。
2。分子の混合:
*溶解のプロセスには、溶質分子と溶媒分子の混合が含まれます。この混合は、システムの可能な微小状態の総数が増加し、最終的にエントロピーを増加させます。
3。水素結合:
*水素結合が有意である場合(たとえば、水に糖を溶解する)、溶質分子と溶媒分子の間に新しい水素結合の形成がエントロピーの増加に寄与する可能性があります。
4。イオン化:
*イオン化合物が溶解すると、イオンに解離し、溶液中の独立した粒子の数が増加するため、エントロピーをさらに増加させる可能性があります。
エントロピーの変化に影響する要因:
* 溶質および溶媒特性: 溶質と溶媒(極性、サイズ、形状)の性質は、エントロピーの変化の程度を決定する上で重要な役割を果たします。
* 濃度: 分子には移動するスペースが増えるため、溶解時のエントロピーの変化は低濃度で大きくなります。
* 温度: エントロピーは一般に、温度の上昇とともに増加します。
全体として、溶解時のエントロピーの変化は、複数の要因の影響を受ける複雑なプロセスです。しかし、一般的な傾向は、溶質を溶解すると、分子障害の増加と分子の混合によりエントロピーが増加することです。