その分子形態の酸素(o₂):
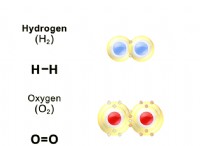
* 非極性: 酸素は二原子分子(O₂)として存在し、2つの酸素原子が電子を均等に共有します。これにより、電子密度が対称的に分布し、分子が非極性になります。
水中の酸素(H₂O):
* 極: 酸素が水素と反応して水を形成すると、物事は大幅に変化します。
* 不平等な共有: 酸素は水素よりもはるかに電気陰です。これは、酸素がO-H結合の共有電子をより強く引っ張っていることを意味します。
* 部分料金: その結果、水中の酸素原子は、共有電子でより多くの時間を費やすため、部分的な負電荷(Δ-)を発症します。 ある程度の電子密度を失った水素原子は、部分的な正電荷(Δ+)を発症します。
* 曲がった形: また、水分子は曲がった形状を採用し、その極性をさらに高めます。
概要:
分子酸素から水への変換は、極性の大幅な変化をもたらします。酸素は、非極性分子の一部から、極性分子の中心原子になります。この極性の変化は、多くの物質を溶解して良好な溶媒として機能するなど、水のユニークな特性にとって重要です。