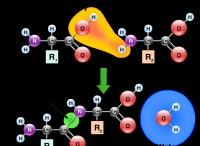
酸化数の理解
* 酸化数 分子またはイオンで電子を追跡する方法です。それらは、すべての結合がイオン性である場合、原子が持つ仮想電荷を表します。
* 酸化数を割り当てるためのルール:
*元素形式の要素の酸化数は0です。
*単原子イオンの酸化数はその電荷に等しくなります。
*ほとんどの化合物の酸素数は-2です(過酸化物を除く、-1)。
*ほとんどの化合物の酸化数は+1です(金属水素化物を除く、-1です)。
*中性分子の酸化数の合計は0です。
*多原子イオンの酸化数の合計は、イオンの電荷に等しくなります。
ヒドラジン(n₂h₄)に規則を適用する:
1。水素の酸化数: ヒドラジンでは、水素は窒素に結合しているため、酸化数は+1です。
2。 xを窒素の酸化数とします: ヒドラジンには2つの窒素原子があるため、窒素の総酸化数は2倍です。
3。酸化数の合計: ヒドラジンの酸化数の合計は、ゼロに等しくなければなりません:2x + 4(+1)=0
4。 x:を解決します 2x + 4 =0 => 2x =-4 => x =-2
したがって、ヒドラジンの窒素の酸化数は-2です。