電気伝導率におけるイオンの役割
* 電気は荷電粒子(イオン)によって運ばれます。 溶液では、これらのイオンは、物質が溶解して成分イオンに解離(分解)すると生成されます。
* 強酸と塩基は溶液中に完全にイオン化します。 これは、高濃度の遊離イオンを生成することを意味します。
* 弱酸と塩基は溶液中に部分的にのみイオン化します。 それらは、より低い濃度の遊離イオンを作成します。
導電率への接続
* 高いイオン濃度=導電率が高い。 溶液中に存在するイオンが多いほど、電流が流れやすくなります。
* 低イオン濃度=導電率が低い。 イオンが少ない溶液は、電気の流れに対してより多くの耐性を提供します。
例
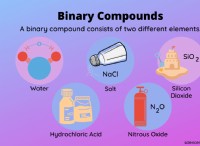
* 塩酸(HCl)は強酸です。 水に溶けると、H+とcl-イオンに完全に解離します。 これにより、高濃度のイオンが生成され、導電率が高くなります。
* 酢酸(CH3COOH)は弱酸です。 溶液中に部分的にのみイオン化し、H+およびCH3COOイオンが少ない数字を生成します。イオン濃度が低いと、導電率が低下します。
要約
強酸と弱酸/塩基の重要な違いは、その程度のイオン化にあります。強酸と塩基は、はるかに大きな遊離イオンのプールを生成し、効率的な電気伝導を可能にします。イオン化が限られている弱酸と塩基は、イオンが少なくなり、電気伝導率が低下します。