これが重要な理由です:
* 反応性: 2つの原子価電子を持つことは、これらの電子を容易に失い、+2カチオンを形成することを意味します。これにより、特に酸素やハロゲンなどの非金属では、非常に反応性が高くなります。
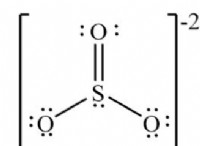
* 結合: +2イオンを形成する傾向は、非金属とのイオン結合につながり、酸化物、塩化物、硫酸塩などのイオン化合物が形成されます。
* 金属文字: ベリリウムとカルシウムはどちらも金属であり、光沢、閉鎖性、導電率などの特性を示しています。
ただし、それらの反応性には次のような違いがあります。
* 原子サイズ: カルシウムはベリリウムよりも大きく、その原子価電子は核から遠く、除去しやすいことを意味します。これにより、カルシウムはベリリウムよりも反応性が高くなります。
* 電気陰性度: カルシウムはベリリウムよりも電気陰性が少ないため、電子を失う可能性が高くなります。
全体として、ベリリウムとカルシウムは同様の電子構成のために同様の化学的特性を共有しますが、その反応性やその他の特性は、原子サイズと電気陰性度の違いにより異なります。