* 分子形状と双極子モーメント:
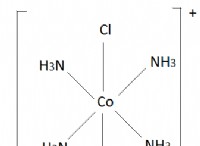
* クロロホルム: クロロホルムには、中心炭素原子に付着した高電気陰性塩素原子を備えた四面体幾何学があります。これにより、かなりの双極子モーメントが作成され、分子極が発生します。
* 酢酸エチル: 酢酸エチルはより複雑な構造を持っています。極結合(C =O、C-O)がありますが、分子の全体的な形状は、これらの双極子が互いに部分的にキャンセルするようなものです。これにより、クロロホルムと比較して全体的な双極子モーメントが小さくなります。
* 水素結合:
* クロロホルム: クロロホルムには、酸素や窒素などの高電気陰性原子に結合した水素原子はありません。これは、水素結合を形成できないことを意味します。
* 酢酸エチル: 酢酸エチルには、水素結合に関与できるカルボニル基(C =O)が含まれています。ただし、この相互作用は、クロロホルムの全体的な双極子モーメントよりも弱いです。
要約: 両方の分子には極性がありますが、塩素原子から強い双極子モーメントを持つクロロホルムの四面体幾何学は、酢酸エチルよりも極性になります。水素結合を形成する能力は、必ずしも分子をより極性にするとは限りません。