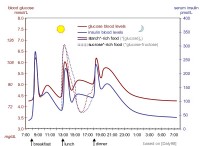
電解質の理解
電解質は、水に溶解すると、電気を伝達できるイオン(荷電粒子)を生成する物質です。
重要な特性:
* イオン化合物: 電解質は通常、イオン化合物です。これらの化合物は、正の帯電イオン(カチオン)と負に帯電したイオン(アニオン)の間の静電引力によって形成されます。
* 水への溶解度: 彼らは、電流を運ぶイオンを放出するために水に溶解する必要があります。
例:
* naCl(塩化ナトリウム): 水中でna+およびcl-イオンに溶解して、電解質になります。
* KCl(塩化カリウム): 水中でk+とcl-イオンに溶解して、電解質になります。
* cacl2(塩化カルシウム): Ca2+および2clイオンに水に溶解して、電解質になります。
フォーミュラから電解質の識別:
1。イオン化合物を探してください: 式には、金属(陽イオン)と非金属(負のイオン)または多原子イオンを含める必要があります。
2。溶解度を考慮してください: ほとんどのイオン化合物は電解質ですが、一部はわずかに溶けたり、水に不溶性です。
確認したい特定の式があるかどうかを教えてください。電解質を表すかどうかを判断するのに役立ちます!