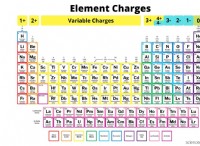
覚えておくべきルール:
*その元素状態の元素の酸化数は0です。
*酸素の酸化数は通常-2ですが、それは-1である過酸化物(h₂o₂など)を除きます。
*水素の酸化数は通常+1ですが、それは-1である金属水素化物(NAHのような)を除きます。
*中性化合物の酸化数の合計は0です。
*多原子イオンの酸化数の合計は、イオンの電荷に等しくなります。
* ルールの適用:
*酸素の酸化数は-2です。
*Agno₃には3つの酸素原子があるため、酸素からの総寄与は-6です。
*硝酸(no₃⁻)は、-1の電荷を持つ多原子イオンです。
* -6の酸素のバランスをとり、全体的な電荷-1にするには、窒素(n)の酸化数は+5でなければなりません。
*化合物全体をニュートラルにするには、銀(AG)には+1の酸化数が必要です。
* したがって、酸化数はです
* AG:+1
* N:+5
* O:-2