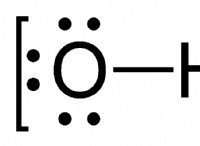「基本」を理解する
* basicity 酸中の交換可能な水素イオン(H⁺)の数を指します。
* Monobasic 酸が分子ごとに1つのH×イオンを寄付できることを意味します。
* dibasic 酸は分子ごとに2つのH培地を寄付できることを意味します。
化合物の分析
* kh₂po₄(リン酸二水素カリウム):
*この化合物では、1つの水素イオン(H⁺)のみが容易に置き換えられます。他の2つの水素イオンは、リン酸塩基に対してより強く結合しています(po₄³⁻)。これがそれが単相性である理由です。
* k₂hpo₄(リン酸カリウム):
*この化合物には、2つの交換可能な水素イオンがあります。水に溶解すると、分子ごとに2つのH⁺イオンが放出され、二等分が発生する可能性があります。
構造の視覚化
このように考えてみてください:
* kh₂po₄: リン酸基(PO₄³⁻)には、水素に付着する可能性がある3つの酸素があります。 この化合物では、2つの酸素が水素をしっかりと保持していますが、3番目の酸素は水素をHイオンとして放出できます。
* k₂hpo₄: ここでは、リン酸塩基には1つの水素しか付着しておらず、2つの酸素が水素イオンをH⁺として放出するために利用可能です。
キーポイント: 交換可能な水素イオンの数は、酸の塩基性を決定します。