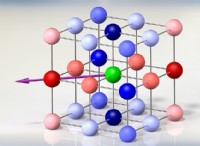
1。 固体(結晶)
* 導電率が低い: 固体状態では、イオン化合物には結晶格子構造があります。 イオンは、強力な静電力によって固定位置に保持されます。
* なぜ? イオンは自由に動くことができません。 彼らが電荷を運んでいる間、彼らが移動できないことは電流の流れを防ぎます。
2。 溶融(液体)状態
* 高い導電率: 溶けると、イオン化合物は液体になります。結晶格子のイオンを保持する静電力は弱くなります。
* なぜ? イオンは液体全体で自由に移動できるようになりました。荷電粒子のこの可動性により、電流の流れが可能になります。
3。 水に溶解した(水溶液)
* 高い導電率: 水に溶解すると、イオン化合物はその構成イオンに解離します。水分子はイオンを囲み、それらを効果的に分離し、自由に動かすことができます。
* なぜ? 溶液中に遊離イオンが存在すると、電流の流れが可能になります。 水は溶媒として機能し、荷電粒子の動きを促進します。
要約
イオン化合物の電気伝導率の重要な要因は、イオンの可動性です。
* ソリッド: イオンは固定されており、導電率が低くなっています。
* 溶け/溶解: イオンは自由に移動し、導電率が高くなります。
例:
塩化ナトリウム(NaCl)はイオン化合物です。その固体形態(テーブルソルト)では、電気の導体が貧弱です。水に溶けたり溶けたりすると、ナトリウム(Na+)と塩化物(Cl-)イオンが自由に移動できるため、良好な導体になります。