* 水素ガスの形成: マグネシウムと塩酸の間の反応は、塩化マグネシウム(MgCl₂)と水素ガス(H₂)を生成します。
`` `
mg(s) + 2hcl(aq)→mgcl₂(aq) +h₂(g)
`` `
* 水素ガスの脱出: 生産される水素ガスは、空気よりも軽い無色で無臭のガスです。それは大気に逃げます。
* 見かけの質量損失: 水素ガスが失われるため、反応混合物の総質量が減少するように見えます。ただし、質量は実際には保存されています。不足している質量は、逃げた水素ガスに含まれています。
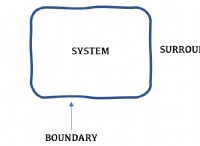
重要な注意: 反応混合物の質量は減少しているように見えますが、システムの総質量(脱出ガスを含む)は一定のままであり、質量の保存法則を支持します。