その理由は次のとおりです。
* 電気陰性度: これは、結合内で電子を引き付ける原子の能力を測定します。
* 同様の電気陰性度: 2つの原子間の電気陰性度の差が小さい(通常は0.5未満)、それらは比較的等しく電子を共有します。
* 極性共有結合: 電子が共有されている間、わずかに高い電気陰性度のある原子は電子をそれ自体に近づけます。これにより、その原子の近くにわずかな負電荷が生じ、他の原子の近くにわずかな正電荷が生じ、双極子モーメントが形成されます。
例:
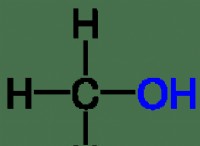
*メタン(CH4)の炭素(C)と水素(H)の間の結合は、極性結合結合です。炭素は水素よりも電気陰性度がわずかに高いため、結合内の電子は炭素原子にわずかに近く、わずかに陰性で水素がわずかに陽性になります。
注:
*電気陰性の差が大きい場合(通常は1.7より大きい)、イオン結合が形成されます。
*電気陰性の差がゼロの場合、純粋な共有結合が形成され、電子は完全に均等に共有されます。