ここに、共有結合が分子物質で普及している理由は次のとおりです。
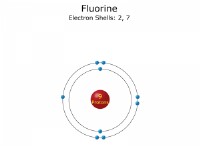
* 電子の共有: 2つの原子が電子を共有すると、共有結合が形成されます。この共有により、両方の原子が安定した電子構成を実現できます。これは、化学的安定性に不可欠です。
* 非金属: 分子物質は通常、非金属原子の組み合わせによって形成されます。非金属は、安定した構成を実現するために電子を獲得する傾向があります。共有結合を介して電子を共有することは、非金属がこの安定性を達成するためのよりエネルギー的に好ましい方法です。
* 離散ユニット: 分子物質は、異なる個々の分子として存在します。これらの分子は共有結合によって結合され、分子自体に強い魅力を生み出します。
共有結合を伴う分子物質の例:
*水(h₂o)
*二酸化炭素(co₂)
*メタン(ch₄)
*グルコース(c₆h₁₂o₆)
ルールの例外:
ほとんどの分子物質は共有結合によってまとめられていますが、いくつかの例外があります。
* イオン化合物: これらの化合物は、正の帯電イオン(カチオン)と負に帯電したイオン(アニオン)の間の静電引力によって形成されます。これらの化合物は分子と見なすことができますが、共有結合によって結合されていません。例は、塩化ナトリウム(NaCl)です。
* 金属物質: これらの物質は、構造全体に電子が非局在化されている金属原子の格子で構成されています。それらは分子と見なすことができますが、従来の共有結合を形成しません。例は金(AU)です。
要約:
共有結合は、非金属原子が電子共有を通じて安定した電子構成を実現できるため、分子物質に見られる最も一般的なタイプの結合です。ただし、イオンおよび金属物質など、この規則には例外があります。