水(h₂o)
* なぜそれが極性であるか: 酸素原子は水素原子よりも電気陰性であり、電子密度の不均一な分布をもたらし、双極子モーメントを作成します。
その他の一般的な例:
* エタノール(c₂h₅oh) :ヒドロキシル基(OH)は非常に極性です。
* アンモニア(nh₃) :窒素原子は、水素原子よりも電気陰性です。
* フッ化水素(HF) :フッ素は最も電気陰性の要素であり、強い双極子モーメントにつながります。
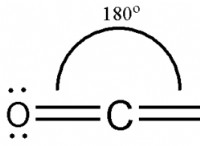
* 二酸化炭素(CO₂) :極結合がありますが、分子は線形で対称的であり、双極子がキャンセルされ、非極性分子が発生します。
* アセトン(Ch₃coch₃) :カルボニル基(C =O)は極性であり、アセトンを極分子にします。
* メタノール(ch₃oh) :ヒドロキシル基(OH)はメタノール極を作ります。
* グルコース(c₆h₁₂o₆) :多くの極性ヒドロキシル基(OH)が極性に寄与しています。
無機極分子:
* 塩化水素(HCl)
***二酸化硫黄(so₂)
* 硝酸(hno₃)
重要な注意:
極性は、分子中の原子間の電気陰性度と分子の形状によって決定されます。 分子に極結合が含まれている場合でも、形状が対称で、双極子がキャンセルする場合、分子は非極性になります。
他の極性分子を溶解する能力のように、極性分子の特性についてもっと知りたいですか?