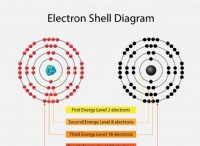
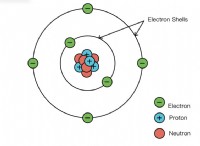
* イオン結合: 塩はイオン化合物です。これは、ナトリウム(Na)と塩素(Cl)が共有化合物の分子のように物理的に結合していないことを意味します。代わりに、ナトリウム原子は電子を失い、正に帯電したナトリウムイオン(Na+)になり、塩素原子は電子を獲得して負に帯電した塩化物イオン(CL-)になります。これらのイオンは、強力な静電力によって結合されています。
* 電気分解: 要素を分離するには、これらのイオン結合を破る必要があります。これは、電解と呼ばれるプロセスを通じて行われます。電気分解は電流を使用して化学反応を強制します。
* それがどのように機能するか:
*液体塩は、電極を備えた電解細胞に入れられます。
*電流は、正に帯電したナトリウムイオンを強制し、負に帯電したカソードに移動し、そこで電子を獲得してナトリウム金属になります。
*負に帯電した塩化物イオンは、積極的に帯電したアノードに移動し、そこで電子を失い、塩素ガスになります。
要約:
*ナトリウムと塩素を液体塩から物理的に分離することはできません。
*電気分解は要素を分離する唯一の方法であり、イオン結合を破壊し、イオンを元素形式に変換することが含まれます。
重要な注意: 塩の電気分解は複雑なプロセスであり、適切な機器と知識で安全に処理することが重要です。