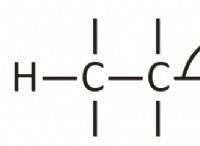その理由は次のとおりです。
* 電気陰性度: 非金属は電気陰性度が高いため、電子に強い魅力があります。これにより、電子を放棄してイオン結合を形成する可能性が低くなります。
* 電子の共有: 電子を伝達する代わりに、非金属は電子を共有して、外側の殻に安定したオクテット(8電子)を実現します。この共有は共有結合を作成します。
共有結合に関与する原子の例:
* 水素(H): 他の水素原子(H-H)と酸素(H-O)や炭素(C-H)などの非金属と共有結合を形成します。
* 酸素(O): 共有結合は、それ自体(O =O)および炭素のような他の非金属(C =O)と形成されます。
* 炭素(c): 水素、酸素、窒素など、他の多くの非金属と共有結合を形成します。
* 窒素(n): 共有結合は、それ自体(NκN)および水素(N-H)や酸素(N-O)などの他の非金属と形成されます。
キーテイクアウト: 共有結合は、安定した電子構成を実現するために電子を共有するため、主に非金属間で発生します。