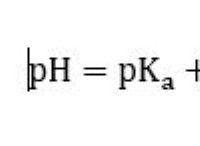分子
* フォーム間: 非金属(および時にはメタロイド)
* ボンドタイプ: 共有結合。これは、原子が電子を共有して安定した外側シェルを達成することを意味します。
イオン化合物
* フォーム間: 金属と非金属
* ボンドタイプ: イオン結合。これは、1つの原子(金属)が電子を失い、正の帯電イオン(陽イオン)になり、もう1つの原子(非金属)が電子をゲインして負に帯電したイオン(アニオン)になることを意味します。 これらの反対に帯電したイオンは、互いに静電的に引き付けます。
重要な違い
* 共有と伝達電子: 分子には電子の共有が含まれますが、イオン化合物は電子の伝達を伴います。
* 結合のタイプ: 分子の共有結合、化合物のイオン結合。
* 物理的特性: 分子は室温のガスまたは液体である傾向がありますが、イオン化合物は通常、融点が高い固体です。
例
* 分子: 水(h₂o)、二酸化炭素(CO₂)、メタン(ch₄)
* イオン化合物: テーブルソルト(NaCl)、炭酸カルシウム(Caco₃)、塩化カリウム(KCL)