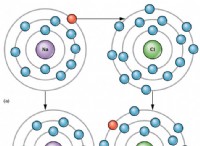
過酸化水素は、式H ₂O ₂を持つ化合物です。純粋な形では、非常に薄い青色の液体であり、優れた酸化剤および還元剤として使用されます。過酸化水素は、産業排水の公害防止処理に使用されています。過酸化水素は、過酸化物結合と呼ばれる単一の共有結合によって結合された 2 つの酸素原子で構成される非平面分子です。
過酸化水素の構造
<オール>過酸化水素の調製
実験準備
<オール>過酸化ナトリウムから (Merck's Process):
この実験室での準備方法では 、氷で覆われ、定期的に攪拌されている弱硫酸(20%)溶液(Na2SO4の結晶)に過酸化ナトリウムを微量加えます。溶液がさらに冷却されると 10H2O が発生し、それらをろ過することができます。
Na2O2+H2SO4→Na2SO4+H2O2
<オール>過酸化バリウムから:
20% の氷冷硫酸溶液を使用して、氷冷水で生成された水和過酸化バリウム (BaO2.8H2O) ペーストを硬化させます。外観が白色の BaSO4 沈殿物は、ろ過を使用して除去されます。 H2O2 の約 5% のみが溶液に残ります。
BaO2⋅8H2O + H2SO4→BaSO4(白色ppt) + H2O2 + 8H2O
硫酸バリウムが H2O2 の周囲に保護コーティングを形成し、化学反応の継続を妨げるため、このアプローチは効果的ではありません。 Ba2+ イオンは、溶液中の過酸化水素を徐々に分解します。その結果、このソリューションは長期保管には適していません。硫酸の代わりに、リン酸がこれをテストするために使用されます。 Ba2+ イオンが存在しない場合、発生するリン酸バリウムは完全に沈殿し、過酸化水素の分解のリスクはありません。
3BaO2⋅8H2O + 2H3PO4 → Ba3(PO4)2(ppt) + 24H2O + 3H2O2
産業準備
市販の調理法はこちら
<オール>セル内で 50% の硫酸溶液を電気分解します。アノードはペルオキソ二硫酸を生成し、これによりカソードで水素が放出されます。
H2SO4 → HSO4– + H+
アノード: HSO4– → H2S2O8 (過酸化硫酸) + 2e–
カソード: 2H+ + 2e– → H2
細胞内の過酸化硫酸が抽出され、水で分解されて過酸化水素が生成されます。
H2S2O8 + 2H2O → 2H2SO4 + H2O2
高沸点の硫酸は蒸留しませんが、過酸化水素は蒸留します。過酸化水素の生成は、硫酸アンモニウムと硫酸の同量混合物を電気分解することで促進できます。
過酸化水素は、アノードで生成された過酸化硫酸アンモニウムを水で凝縮することによって得られます。
(NH4)2S2O8 + 2H2O → 2NH4HSO4(硫酸水素アンモニウム) + H2O2
- 2-エチル アントラキノンの助けを借りて
パラジウム触媒の存在下で、ベンゼンに溶解した 2-エチル アントラキノンを介して水素ガスが輸送されます。 2-エチルアントラキノンに分解される。次に、空気は、2-エチル アントラキノン、ベンゼン、およびシクロヘキサノールの混合物でポンピングされます。 2-エチル アントラキノンが酸化されて過酸化水素に戻ると、過酸化水素が生成されます。
- イソプロピル アルコールは酸化されています :
この商用の準備方法の下で 少量の過酸化水素をイソプロピルアルコールと混合すると開始剤として作用します。酸素は、約 340K で少量の圧力で溶液を透過します。酸化反応の結果、アセトンと過酸化水素が発生します。
CH3CHOHCH3(イソプロピルアルコール) + O2 → CH3COCH3(アセトン) + H2O2
過酸化水素の性質
過酸化水素の性質
- 最も純粋な形の過酸化水素は、ほとんど無色 (非常に淡い青色) です。
- その沸点は摂氏 150.2 度と計算されており、これは水の沸点より摂氏 50 度以上高いです。
- 過酸化水素の融点は摂氏マイナス 0.43 度です。
- 水の中で水和し、あらゆる量で均一な混合物を生成します。
- 過酸化水素のモル質量は 34.0147 g/mol です。
- 少しきつい匂いがあります。
- 水溶液の密度は 1.11 g/cc で、純粋な形の密度は 1.450 g/cc です。
結論
これで、市販の調理方法のまとめです .過酸化水素は過酸化物の最も基本的な種類です。物を安全に保つために水溶液に使用される無色の液体です。漂白剤としてだけでなく、消毒剤としても使用されます。気体の過酸化水素は、地球の大気中で光化学プロセスによって生成されます。殺菌剤と漂白剤の両方の役割を果たします。華氏 298 度では酸性で、pH は 6 から 7 です。