* 原子は化学反応で作成または破壊されません: 彼らは単に自分自身を異なる組み合わせに再配置します。
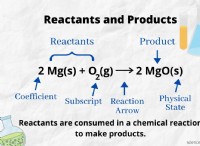
* バランスの取れた方程式はこれを反映しています: 各化学式の前の係数は、関与する分子またはモルの数を表します。 これらの係数は、方程式の両側に各タイプの原子の数が表示されるように調整されます。
例:
水素と酸素の水を形成する反応:
不均衡な方程式: h₂ +o₂→h₂o
バランスの取れた方程式: 2h₂ +o₂→2h₂o
* 不均衡: この方程式は、反応物側に2つの水素原子と2つの酸素原子を示していますが、生成物側には2つの水素原子と1つの酸素原子のみを示しています。
* バランス: この方程式は、4つの水素原子(2 x 2)と両側に2つの酸素原子を示しており、原子が失われたり稼いだことを示しています。
したがって、バランスのとれた化学式により、反応物の総質量が生成物の総質量に等しく、質量の保存法則と一致することが保証されます。