これが故障です:
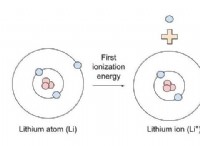
* イオン結合: 転送が含まれます ある原子から別の原子への電子の。これにより、互いに引き付けられ、結合を形成する反対の電荷でイオン(帯電した原子)が生成されます。
* 共有結合: 共有が含まれます 原子間の電子の。共有電子は両方の原子の核に引き付けられ、強い結合が生じます。
重要な違い:
* 電子移動対共有: イオン結合には電子の完全な移動が含まれますが、共有結合には共有が含まれます。
* イオンの形成: イオン結合はイオンの形成をもたらしますが、共有結合はそうではありません。
* 要素の種類: イオン結合は通常、金属と非金属間で発生しますが、共有結合は非金属間で発生します。
例:
* イオン: NaCl(塩化ナトリウム) - ナトリウム(Na)は塩素(Cl)に電子を失い、互いに引き付けるNa+およびCl-イオンを形成します。
* 共有結合: H2O(水) - 酸素(O)は、2つの水素(H)原子で電子を共有し、安定した分子を形成します。
要約: 価電子の共有は、イオン結合ではなく、共有結合の定義的な特徴です。