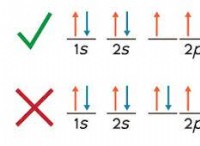
1。電子構成:
* 価電子: 最も外側のシェル(価電子)の電子の数が主要な要因です。要素は、最も外側のシェルに安定したオクテット(8電子)を達成するために電子を失ったり獲得したりする傾向があります。
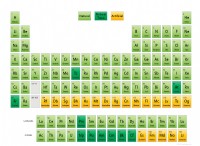
* グループ番号: 主なグループ要素の場合、グループ数は多くの場合、価電子の数に対応し、潜在的な酸化状態を決定するための良い出発点を提供します。
* dブロック要素: 遷移金属は、結合にD-電子が関与しているため、さまざまな酸化状態を持っています。
2。電気陰性度:
* エレクトロポジティブ要素: 電気陰性度が低い(金属など)の要素は、電子を失い、陽性の酸化状態を形成する傾向があります。
* 電解要素: 電気陰性度が高い(例えば、非金属)の元素は、電子を獲得し、負の酸化状態を形成する傾向があります。
3。定期的な傾向:
* イオン化エネルギー: イオン化エネルギーが低い元素は、容易に電子を失い、陽性の酸化状態を支持します。
* 電子親和性: 電子親和性が高い元素は、容易に電子を獲得し、負の酸化状態を支持します。
4。化学環境:
* ボンディングパートナー: 要素の結合パートナーの性質は、その酸化状態に影響を与える可能性があります。たとえば、酸素はしばしば他の元素をより高い酸化状態にします。
* 化学反応: 特定の反応条件は、元素の酸化状態を決定できます。
5。一般的な酸化状態:
* グループ1および2: それぞれ+1と+2。
* グループ17: -1(ハロゲン)。
* グループ16: -2(酸素、硫黄など)。
* グループ15: -3(窒素、リンなど)。
その他の要因:
* サイズ: より大きな原子は電子をより簡単に失う傾向があり、陽性の酸化状態を支持します。
* 核電荷: より高い核電荷を使用すると、電子を除去するのが難しくなり、より高い酸化状態を支持します。
最も可能性の高い酸化状態を決定する:
絶対的なルールはありませんが、これらの要因を分析して、最も可能性の高い酸化状態を予測できます。
1。要素の電子構成とグループ番号を考慮してください。
2。その電気陰性度と周期表の位置を評価します。
3。その結合パートナーと反応条件を考慮してください。
4。特定のグループの一般的な酸化状態を参照してください。
酸化状態は常に固定されているわけではなく、化学環境によって異なる場合があることを忘れないでください。