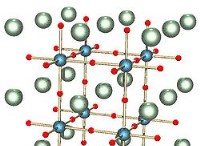
* solid(ice): 固体状態では、水分子は通常の結晶構造にしっかりと詰め込まれています。水分子間の水素結合は強く、固定位置に保持され、高密度と分子が互いに非常に近いことにつながります。
* 液体(水): 液体の水では、水素結合は弱く、絶えず破損し、改革しています。これにより、分子がより自由に動き回ることができ、氷と比較して分子間の密度が低く距離が長くなります。
* ガス(水蒸気): 気体状態では、水分子は広く分離され、迅速に移動し、それらの間の非常に弱い相互作用があります。
したがって、固体 水の相により、個々の分子が最も近くになることができます。