* 電気陰性度: 非金属は比較的高い電気陰性度であり、それは電子を強く引き付けることを意味します。 2つの非金属が電子を共有する場合、電気陰性の差は電子を完全に伝達するほど大きくなく、共有電子ペアにつながります。
* 電子の共有: 非金属は、安定した電子構成を実現するために、いくつかの電子を獲得する必要があることがよくあります(貴重なガスなど)。電子を共有すると、完全な電子を失ったり獲得したりすることなく、外側のシェルを完成させることができます。
一般的に共有結合を形成する要素の例:
* グループ14: 炭素(c)、シリコン(SI)
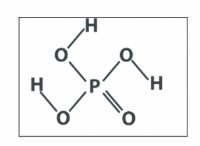
* グループ15: 窒素(N)、リン(P)
* グループ16: 酸素(O)、硫黄(S)
* グループ17: フッ素(F)、塩素(Cl)、臭素(BR)、ヨウ素(I)
例外:
非金属は一般に共有結合を形成しますが、いくつかの例外が存在します。
* 水素(H): それは非金属ですが、しばしば非金属との共有結合を形成し、金属とのイオン結合を形成します。
* メタロイド: 一部のメタロイド(ホウ素(B)やシリコン(SI)など)は、共有結合を形成できます。
要約: 非金属は、電気陰性度と電子分配の必要性により、共有結合を形成するための最も一般的な要素です。