1。イオン:
* カチオン: 原子が電子を失うと形成された正に帯電したイオン。これらは通常、ナトリウム(Na+)やカルシウム(Ca2+)などの金属です。
* アニオン: 原子が電子を獲得するときに形成される負に帯電したイオン。これらは通常、塩素(Cl-)や酸素(O2-)などの非金属です。
2。静電引力:
*陽イオンと陰イオンの反対の電荷が互いに強く惹かれ、イオン結合を形成します。
*この強い魅力は、硬い結晶構造でイオンを一緒に保持します。
3。クリスタル格子:
*イオン化合物は、結晶格子と呼ばれるイオンの3次元配置として存在します。
*この構造により、各イオンが反対に帯電したイオンに囲まれていることが保証され、静電引力が最大化されます。
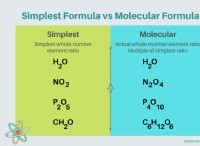
4。フォーミュラユニット:
*結晶格子のイオンの比を表すイオン化合物の最小単位は、式ユニットと呼ばれます。
*たとえば、NaCl(塩化ナトリウム)には、結晶格子のすべての塩素イオン(Cl-)に1つのナトリウムイオン(Na+)があります。
イオン化合物の重要な特性:
* 高融点と沸点: イオン間の強い静電力のため。
* 室温での固体: 硬い結晶構造は、それらが液体やガスであることを防ぎます。
* 水または溶融に溶解したときに電気を伝達: イオンは自由に移動して電荷を運ぶことができるからです。
* 脆性: 硬い結晶構造は、強い力によって簡単に破壊され、化合物が壊れます。
イオン化合物の形成:
イオン化合物は、金属(電子を失う傾向がある)が非金属(電子を獲得する傾向がある)と反応するときに形成されます。この電子移動は、反対に帯電したイオンを作成し、互いに引き付けて化合物を形成します。
例:
*ナトリウム(Na)は金属であり、ナトリウムイオン(Na+)になるために1つの電子を失う傾向があります。
*塩素(Cl)は非金属であり、1つの電子を獲得して塩化物イオン(Cl-)になる傾向があります。
* Na+とclの間の静電引力は、イオン化合物の塩化ナトリウム(NaCl)を形成します。
要約すると、イオン化合物は、反対に帯電したイオン(陽イオンと陰イオン)間の静電引力によって形成されます。これらのイオンは特定の結晶格子に配置され、一意の特性を持つ化合物を作成します。