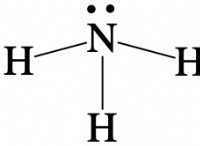
* 電子構成: 塩素には17の電子があり、構成は2-8-7です。これは、最も外側のシェル(価数シェル)に7つの電子があることを意味します。
* オクテットルール: 原子は、最も外側のシェルに8つの電子を持つ貴族のような安定した電子構成を実現するよう努めています(ヘリウムを除く2つのヘリウムを除く)。
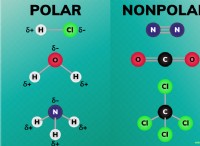
* イオン結合: 塩素は非常に電気陰性であり、電子に強い魅力を持っていることを意味します。安定したオクテットを達成するために、1つの電子を容易に獲得して負に帯電したイオン(アニオン)になります。
したがって、塩素がイオンを形成すると、1つの電子を獲得してcl⁻(塩化物イオン)になります。