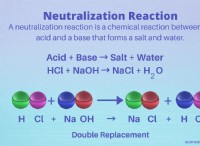
これが故障です:
1。構造: Imidesには、窒素原子に2つのカルボニル基が付いています。これらのカルボニル基は高度に偏光されており、炭素原子は電子不足で、酸素原子は電子が豊富です。
2。電子撤退: カルボニル基の電子吸引効果は、窒素原子から電子密度を引き離します。これにより、窒素原子がより陽性であるため、プロトン(H+)を寄付する可能性が高くなります。
3。共鳴安定化: 陽子が失われたときに窒素原子に形成される負電荷は、カルボニル基との共鳴によって非局在化することができます。この共鳴安定化により、脱プロトン化されたイミードアニオンがより安定し、酸性度がさらに促進されます。
4。誘導効果: カルボニル基の誘導効果も酸性度に寄与します。カルボニル基の電子吸引性の性質により、N-H結合がより極性になり、水素原子がより酸性になります。
要約: カルボニル基による電子離脱の複合効果と、結果として生じる陰イオンの共鳴安定化により、イミドが酸性になります。
これが視覚的な表現です:

イミドの酸性度は、イミドの共鳴安定化により、通常、カルボン酸の酸性度よりも弱いことに注意してください。これにより、イミド陰イオンの反応性が低下します。