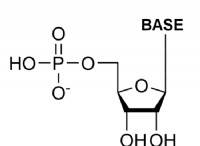
* 構造: リン酸には、リン酸基(PO4)に結合した3つの水素原子があります。これらの水素原子は、非常に陰性酸素原子に付着しています。
* 電気陰性度: 酸素は水素よりも電気陰性です。つまり、H-O結合の共有電子をそれ自体に近づけます。これにより、水素原子が部分的に陽性になります(Δ+)。
* 陽子寄付: 部分的に陽性の水素原子は、プロトン(H+)として比較的簡単に除去されます。 H3PO4が水に溶解すると、1つ、2つ、または3つの陽子すべてを寄付でき、H2PO4-、HPO42-、PO43-などのさまざまなイオンを形成できます。
* brønsted-lowry定義: 酸のブレンステッドローリー定義によれば、陽子(H+)を寄付する物質は酸です。リン酸は陽子を寄付できるため、この定義に適合します。
要約:
H3PO4は、その構造により、水に溶解すると陽子(H+)を簡単に寄付できるため、酸です。このプロトンの寄付は、Brønsted-Lowry理論によると、酸の決定的な特徴です。