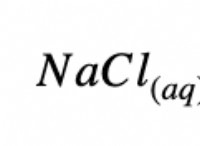極分子:
* 導電率: 極性分子は、一般に電気の導体が貧弱です 純粋な液体または固体の形で。
* 推論:
* 弱い相互作用: 極性分子は、イオン化合物のイオン結合よりも弱い双極子双極子相互作用と水素結合によって結合されます。これらの弱い相互作用は、電気伝導率に必要な荷電粒子の自由な動きを許可しません。
* 遊離イオンなし: 極性分子は、純粋な状態の遊離イオンに容易に解離しません。これは、電気伝導率の要件です。
* 例外:
* ソリューション: 水(または他の極性溶媒)に溶解した極性分子は、良好な導体になる可能性があります。これは、溶媒が極性分子をイオンに分離し、電荷の流れを可能にするためです。
* いくつかの特定のケース: いくつかの極性分子は、一時的なイオンペアを形成する能力や高誘電率を持つことにより、特別な状況のために純粋な状態で電気を導入できます。
イオン化合物:
* 導電率: イオン化合物は、電気の良好な導体です 溶融(液体)または水に溶解する場合(水溶液)。
* 推論:
* 強い相互作用: イオン化合物は、正に帯電したイオンと負に帯電したイオンの間の強い静電力(イオン結合)によって結合されます。これらの力は、極性分子の相互作用よりもはるかに強いです。
* 遊離イオン: イオン化合物が溶融または溶解すると、イオンは自由に動き回り、電荷を運びます。
* 固体状態: イオン化合物は、通常、導体が不十分です イオンは剛体格子構造に閉じ込められており、自由に動くことができないため、固体状態で。
要約:
分子が電気を導入する能力は、主に自由変動荷電粒子(イオン)の存在に依存します。
* イオン化合物 溶けたり溶けたりすると、遊離イオンがあり、それらを良好な導体にします。
* 極分子 一般に、純粋な状態には遊離イオンが不足しているため、導体が貧弱になりますが、極性溶媒に溶解すると導くことができます。
他に質問がある場合はお知らせください!