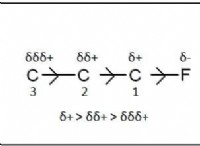
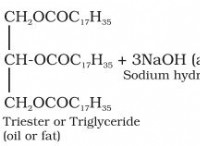イオン化合物の理解
* イオン化合物 金属(亜鉛のような)が電子を非金属に伝達するときに形成します。
* カチオン: 金属は電子を失い、正に帯電したイオンになります。
* アニオン: 非金属は電子を獲得し、負に帯電したイオンになります。
* 中性化合物: 化合物の全体的な電荷は中性でなければなりません。
亜鉛の電荷
亜鉛(Zn)は通常、+2陽イオン(Zn²⁺)を形成します。
比率を見つける
亜鉛を使用して1:2の比率を取得するには、-1電荷でアニオンを形成する非金属が必要です。これは:
* 1つのZn²⁺イオン(+2充電付き)
*料金のバランスを取るには、2つの-1アニオンが必要です
に合う要素
ハロゲン(周期表のグループ17)は、-1アニオンを形成する最も一般的な要素です。これらには以下が含まれます:
* フッ素(f⁻)
* 塩素(cl⁻)
* 臭素(br⁻)
* ヨウ素(i⁻)
例
* フッ化亜鉛(Znf₂): 1つの亜鉛イオン(Zn²⁺)は、2つのフッ化物イオン(2 xf⁻)と結合します
* 塩化亜鉛(Zncl₂): 1つの亜鉛イオン(Zn²⁺)は、2つの塩化物イオン(2 xCl⁻)と結合します。
重要な注意: これらのハロゲンは一般的ですが、特定の条件下で-1電荷を形成する他の要素がある可能性があります。ただし、ハロゲンは、亜鉛と1:2の比率を形成する最も信頼できる要素です。