* ナトリウム(Na) 金属であり、電気陰性度が低いです。これは、安定した電子構成を実現するために、単一の価電子を容易に失うことを意味します。
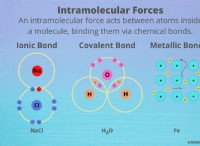
* イオン結合 1つの原子(通常は金属)が別の原子(通常は非金属)に電子を失い、互いに引き付ける反対に帯電したイオンを作成すると形成されます。
これが他のオプションの可能性が低い理由の内訳です:
* 共有結合 原子が電子を共有するときに形を形成します。ナトリウムは、電子を失う傾向が強いため、他の原子と電子を共有することはありません。
* 水素結合 酸素や窒素などの高電気陰性原子に結合した水素原子の間で発生する特定のタイプの双極子双極子相互作用です。ナトリウムは水素結合を形成しません。
例: ナトリウムは塩素(Cl)とのイオン結合を容易に形成して、一般にテーブル塩として知られている塩化ナトリウム(NaCl)を作成します。