その理由は次のとおりです。
* 共有結合: 共有結合では、原子は電子を共有して安定した電子構成を実現します。
* 極: 「極」という用語は、正と負の終わり(磁石のような)の存在を指します。
* 不平等な共有: 電子が1つの原子に向かってより強く引っ張られると、その原子に部分的な負電荷と他の原子に部分的な正電荷が生成されます。電子密度のこの不均一な分布は、結合を極性にします。
極性共有結合の例:
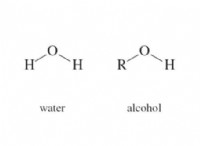
* 水(h₂o): 酸素は水素よりも電気陰性であるため、共有電子を近づけ、酸素に部分的な負電荷と部分的な正電荷を与えます。
* 塩化水素(HCl): 塩素は水素よりも電気陰性であり、極性結合をもたらします。
キーテイクアウト: 共有結合中の原子間の電気陰性度の違いは、結合が極性か非極性であるかを決定します。