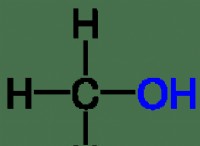
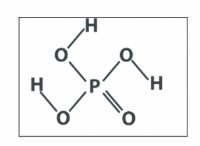
* 酸には水素イオンが必要です: 酸は、溶液中に水素イオン(H+)を寄付する能力によって定義されます。
* 水はニュートラルです: 水(H2O)は中性分子です。それは弱酸と弱い塩基の両方として作用することができますが、真の酸のように水素イオンを容易に寄付することはありません。
* 酸素は酸化剤です: 酸素は非常に反応性のある要素です。他の物質と反応して酸化物を形成することができますが、水素イオンの形成に直接寄与しません。
酸素と水を混ぜるとどうなりますか?
酸素は水に少し溶けます。この溶存酸素は、呼吸に使用されているように、水生寿命に不可欠です。水中の酸素の存在は、酸化反応による他の物質の形成にもつながる可能性がありますが、これらの反応は酸の産生をもたらさない。
酸を作成するには、が必要です
* 水素イオンの源: これは、HCl(塩酸)やH2SO4(硫酸)のような分子であり、水に溶解すると容易に水素イオンを寄付します。
* 溶媒: 通常、水は溶媒として使用されますが、他の溶媒も使用できます。
他に質問がある場合はお知らせください!