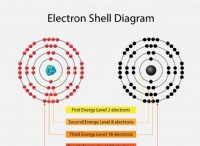
セシウム原子
* ニュートラル: セシウム原子にはニュートラル電荷があります。 55個の陽子(正電荷)と55個の電子(負電荷)が含まれており、電荷のバランスが取れています。
* 電子構成: 電子の完全な外側の殻があります。 電子構成は[xe]6s¹-それが最も外側のシェルに1つの価電子を持っていることを意味します。
* 反応性: セシウムは単一の原子価電子のために非常に反応性があり、陽イオンを形成するために容易に失われます。
セシウムイオン(cs⁺)
* 正電荷: セシウムイオンは、1つの電子を失ったため、正電荷を持っています。現在、55個の陽子と54個の電子があります。
* 電子構成: 電子構成は、Noble Gas Xenon([Xe])と同じになりました。 完全な外側のシェルがあり、より安定しています。
* 層: セシウム原子は単一の原子価電子を簡単に失い、セシウムイオン(CS⁺)になります。これは、セシウムのイオン化エネルギーが非常に低いためです。
要約:
重要な違いは、電子の数と結果として生じる電荷にあります。セシウム原子はニュートラルで1つの原子価電子がありますが、セシウムイオンは1つの電子の損失により正電荷を持ち、安定した電子構成を与えます。