酸化数の理解
* 定義: 酸化数(または酸化状態)は、すべての結合が100%イオンである場合、原子が持つ仮想電荷を表します。
* 電気陰性度: 酸化数の割り当ては、関与する原子の電気陰性度に基づいています。電気陰性度とは、原子が結合中に電子を引き付ける能力です。
酸化数を割り当てるためのルール
1。自由要素: 元素形式の原子の酸化数は常に0です(例:Na、O2、Cl2)
2。単原子イオン: 単原子イオンの酸化数はその電荷に等しくなります。 (例えば、Na + =+1、O2- =-2)
3。フッ素: フッ素は最も電気陰性の要素であり、化合物では常に-1の酸化数があります。
4。酸素: 酸素は通常、それが-1である過酸化物(H2O2など)を除き、陽性である化合物(H2O2など)を除き、陽性(OF2のような)を除き、酸化数を-2にします。
5。水素: 水素は通常、それが-1である金属水素化物(NAHのような)を除き、化合物で+1の酸化数を持っています。
6。酸化数の合計: ニュートラル化合物の酸化数の合計は、ゼロに等しくなければなりません。多原子イオンでは、酸化数の合計はイオンの電荷に等しくなければなりません。
7。グループ1および2: グループ1(アルカリ金属)の元素の酸化数は+1であり、グループ2(アルカリ地球金属)の元素は、化合物の酸化+2の酸化数を持っています。
8。ハロゲン: ハロゲン(グループ17)は通常、-1の酸化数を持っていますが、酸素(CLO2など)または他のハロゲン(BRCLなど)の化合物に陽性の酸化数を持つことができます。
例
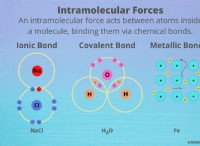
* naCl: ナトリウム(Na)は、塩素(Cl)よりも電気陰性度が低いです。 NAの酸化数は+1(グループ1ルール)で、CLの酸化数は-1です。
* H2O: 酸素は水素よりも電気陰性です。 水素の酸化数は+1であり、酸素の酸化数は-2です。
* K2CR2O7: カリウム(K)の酸化数は+1(グループ1ルール)であり、酸素の酸化数は-2です。 2つのカリウム原子の酸化数の合計は+2であり、7つの酸素原子の合計は-14です。これとのバランスをとるには、2つのクロム原子の酸化数が+12である必要があるため、各クロム原子の酸化数は+6です。
ヒント
* 一般的な酸化数を記憶します: フッ素、酸素、水素、グループ1および2の要素などの元素のルールを知ってください。
* 酸化数の合計ルール:を使用します 化合物内の未知の要素の酸化数を決定するのに役立ちます。
* 練習: 酸化数の割り当てに慣れる最良の方法は、さまざまな例で練習することです。
一緒に作業したい特定の化合物がある場合はお知らせください!