1。塩の性質を理解してください
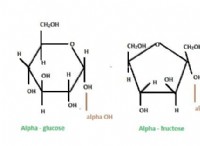
*na₂c₄h₂o₄は、強力な塩基(NaOH)と弱酸(フマル酸、c₄h₄o₄)の中和反応から形成された塩です。
*これは、塩が加水分解を受けることを意味します。ここでは、陰イオン(c₄H₂O₄²⁻)が水と反応して水酸化物イオン(OH⁻)を生成します。
2。加水分解反応を書きます
c₄h₂o₄²⁻(aq) +h₂o(l)⇌hc₄h₃o₄⁻(aq) +oh⁻(aq)
3。アイステーブルをセットアップ
| | c₄h₂o₄²⁻| hc₄h₃o₄⁻|ああ|
| ------------ | ------------ | ------------ | ------------ |
|初期(i)| 1.00 m | 0 | 0 |
|変更(c)| -x | +x | +x |
|平衡(e)| 1.00-x | x | x |
4。加水分解定数(kb)を決定します
*フマレートイオンの塩基イオン化定数であるKBを見つける必要があります。 KA(フマル酸の酸イオン化定数)とKBの関係を使用できます。
KB =kw / ka
* kw(水のイオン製品定数)=1.0 x10⁻¹⁴
* Ka(フマル酸の場合)=9.3 x10⁻⁴
* kb =(1.0 x10⁻¹⁴) /(9.3 x10⁻⁴)=1.1 x10⁻¹¹¹残念
5。 x(水酸化物イオン濃度)を解きます
* kb =[hc₄h₃o₄⁻] [oh⁻] / [c₄h₂o₄²⁻]
* 1.1 x10⁻¹¹=(x)(x) /(1.00 -x)
* KBは非常に小さいため、Xが1.00よりもはるかに小さいと仮定できます。これにより、方程式が簡素化されます。
* 1.1 x10⁻¹¹≈x² / 1.00
*x²≈1.1x10⁻¹¹
*x≈3.3x10⁻⁶m(これは[OH⁻]濃度です)
6。 pohとph を計算します
* poh =-log [oh⁻] =-log(3.3 x10⁻⁶)≈5.48
* ph + poh =14
*pH≈14-5.48≈8.52
したがって、1Mna₂c₄h₂o₄溶液のpHは約8.52です。これは、ソリューションがわずかに基本的であることを示しています。