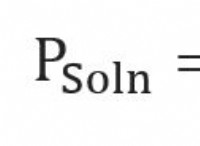Trisの理解
Tris(Tris(ヒドロキシメチル)アミノメタン)は弱い塩基です。 その化学式は(HOCH2)3CNH2です。これは、バッファーとして生化学と分子生物学で一般的に使用されています。
pHの計算
1。平衡反応を書きます:
(HOCH2)3CNH2(AQ) + H2O(L)⇌(HOCH2)3CNH3 +(AQ) + OH-(AQ)
2。 KB値を識別します:
TRISのKB(ベース解離定数)は1.17 x 10^-6です。
3。アイステーブルを設定します(初期、変化、平衡):
| | (HOCH2)3CNH2 | (HOCH2)3CNH3+ |ああ - |
| ------------- | ----------------- | ---------------- | ----------- |
|初期(i)| 0.045 m | 0 | 0 |
|変更(c)| -x | +x | +x |
|平衡(e)| 0.045 -x | x | x |
4。 KB式を書きます:
kb =[(hoch2)3cnh3+] [oh-] / [(hoch2)3cnh2]
5。アイステーブルの平衡値を代用してください:
1.17 x 10^-6 =(x)(x) /(0.045 -x)
6。単純化(x <<0.045を仮定):
1.17 x 10^-6≈x^2 / 0.045
7。 x([oh-]を表す)を解く:
x =√(1.17 x 10^-6 * 0.045)
x≈2.3x 10^-4 m
8。 poh:を計算します
poh =-log [oh-] =-log(2.3 x 10^-4)≈3.64
9。 ph:を計算します
ph + poh =14
pH =14-3.64≈10.36
したがって、0.045 mトリスベース溶液のpHは約10.36です。