共有結合
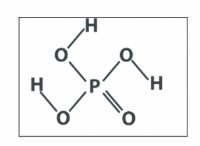
* 共有は思いやりがあります: 共有結合では、原子 *を共有 *電子を共有して、安定した電子構成を実現します(通常、貴族に似ています)。
* 非金属: 共有結合は主に非金属原子間で発生します。
* 平等共有(非極性)または不均等共有(極):
* 非極性共有結合: 電子は原子間で等しく共有されます。
* 極性共有結合: 電子は不均等に共有され、分子のわずかに正でわずかに負の端(双極子)が生成されます。
* 強い債券: 共有結合は比較的強力であり、壊れるのにかなりのエネルギーが必要です。
* 例: 水(H₂O)、メタン(CH₄)、二酸化炭素(CO₂)
イオン結合
* 授与と服用: イオン結合では、1つの原子 *が別の原子に電子を透過し、反対に帯電したイオンを作成します。
* 金属と非金属: イオン結合は通常、金属と非金属の間で発生します。
* 静電引力: 反対に帯電したイオンは互いを強く引き付け、静電結合を形成します。
* 強い債券: イオン結合も、特に固体状態では比較的強力です。
* 例: テーブル塩(NaCl)、酸化マグネシウム(MGO)、塩化カルシウム(Cacl₂)
主要な違いを要約する便利なテーブルです:
|機能|共有結合|イオン結合|
|--------------------|---------------------------------------------------|----------------------------------------------------------|
|電子共有|原子は電子を共有します|原子伝達電子|
|関係する原子|通常、非金属|通常、金属と非金属|
|ボンドタイプ|電子ペアの共有|イオン間の静電引力|
|強さ|強い|特に固体状態では強い|
|例|水(H₂O)、メタン(Ch₄)、二酸化炭素(CO₂)|テーブルソルト(NaCl)、酸化マグネシウム(MGO)、塩化カルシウム(CACL₂)|
もっと詳細や例が欲しいかどうか教えてください!