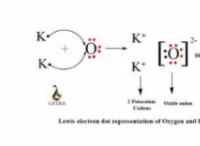
反応:
Zn(no₃)₂(aq) + pb(s)→pb(no₃)₂(aq) + zn(s)
説明:
* 亜鉛(Zn) リード(PB)よりも反応性があります 。これは、亜鉛が電子を失い、陽性イオンを形成する傾向が強いことを意味します。
*反応では、亜鉛はその硝酸塩から導きます 、鉛硝酸鉛(Pb(no₃)₂)および固体亜鉛を形成します 。
*反応は自発的です および発熱 、それが熱を放出することを意味します。
観測:
* 硝酸塩 水に溶けやすく、溶液にとどまります。
* 亜鉛 鉛よりも反応性が低く、ソリッドとして堆積します 鉛の表面。
*色の変化を観察することができます 反応が進むにつれて、反応物の初期濃度に応じて。
注: この反応は、単一の変位反応の典型的な例であり、より反応性のある金属は、その塩からそれほど反応性の低い金属を変位させます。