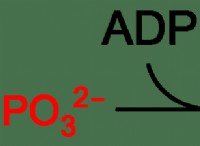
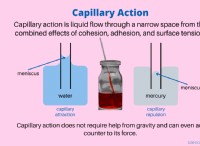
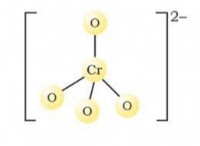
その理由は次のとおりです。
* イオン結合 ある原子が電子を別の原子に完全に透過すると発生します。この伝達により、イオンが生成されます。正に帯電イオン(陽イオン)と負に帯電したイオン(アニオン)です。反対の電荷は互いに強く惹かれ、イオン結合を形成します。
イオン結合は分子間力の最も強いタイプですが、分子間には他のタイプの引力があります。
* 水素結合: これらは、高強性原子(酸素、窒素、またはフッ素など)と近くの分子の電子ペアに共有結合した水素原子との間の強い魅力です。
* 双極子型相互作用: これらは、1つの分子の正の帯電した端が別の分子の負に帯電した端に引き付けられる極性分子間で発生します。
* ロンドン分散部隊: これらは、分子内の電子分布の一時的な変動から生じる弱い魅力です。
これらの力の強さは変化し、物質の全体的な挙動はこれらすべての相互作用の組み合わせ効果に依存することを覚えておくことが重要です。